Jak wynika z badania LIBRETTO-531 selperkatynib poprawia wyniki, w porównaniu do kabozantynibu lub wandetanibu w pierwszej linii leczenia pacjentów z zaawansowanym rakiem rdzeniastym tarczycy z mutacją RET.
Nowy standard opieki
We wspomnianym badaniu III fazy selperkatynib poprawił przeżycie wolne od progresji (PFS), przeżycie wolne od niepowodzenia leczenia (TFFS) oraz przeżycie całkowite (OS).
Według prezentującego badanie dr. Julien Hadoux, MD, PhD, z Gustave Roussy
Wyniki badania wskazują selperkatynib jako nowy standard leczenie w pierwszej linii dla pacjentów z zaawansowanym rakiem rdzeniastym tarczycy z mutacją RET.
Selperkatynib wyniki leczenia
Badanie LIBRETTO-531 (Identyfikator ClinicalTrials.gov: NCT04211337) obejmowało 291 pacjentów z nieoperacyjnym, miejscowo zaawansowanym lub przerzutowym rakiem rdzeniastym tarczycy z mutacją RET, nie leczonych wcześniej inhibitorami kinazy.
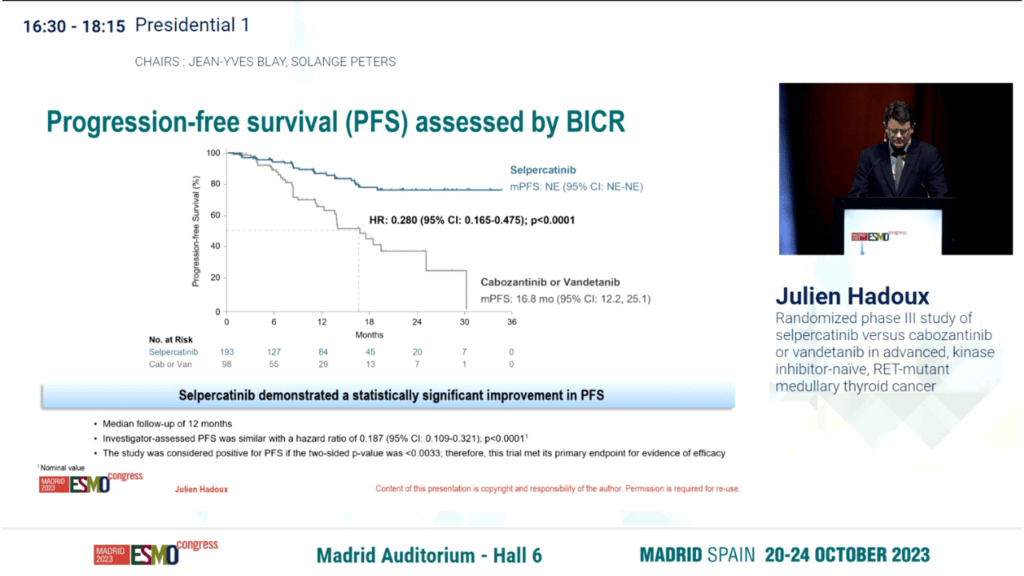
Pacjenci zostali losowo przydzieleni do otrzymania selperkatynibu (n=193) lub leku wybranego przez lekarza spośród kabozantynibu lub wandetanibu (n=98). W przypadku nastąpienia progresji choroby, pacjenci mogli przejść z grupy kontrolnej do grupy otrzymującej selperkatynib. Ostatecznie 77,4% uprawnionych pacjentów (n=24) przeszło na leczenie selperkatynibem.
Średni czas obserwacji dla PFS wynosił 12 miesięcy. Średni PFS, według zaślepionej niezależnej oceny, nie został osiągnięty w grupie selperkatynib i wynosił 16,8 miesiąca w grupie kontrolnej (współczynnik ryzyka [HR], 0,280; 95% CI, 0,165-0,475; P <.0001).
Średni czas obserwacji dla TFFS wynosił 12 miesięcy. Średni TFFS nie został osiągnięty w grupie selperkatynibu i wynosił 13,9 miesiąca w grupie kontrolnej (HR, 0,254; 95% CI, 0,153-0,423; P <.0001).
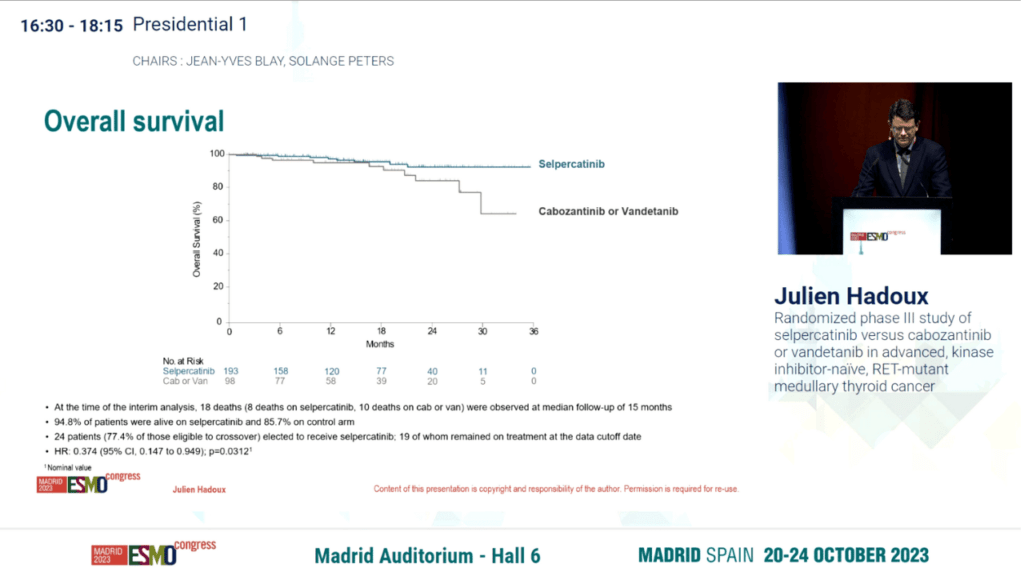
Średni czas obserwacji dla OS wynosił 15 miesięcy. W tym czasie 94,8% pacjentów w grupie selperkatynibu i 85,7% tych w grupie kontrolnej nadal żyło (HR, 0,374; 95% CI, 0,147-0,949; P =.0312).
Bezpieczeństwo leczenia
Wskaźnik zdarzeń niepożądanych (AE) stopnia 3 lub wyższego, które pojawiły się podczas leczenia, wynosił 52,8% w grupie selperkatynibu i 76,3% w grupie kontrolnej. Przerwanie leczenia z powodu zdarzeń nie pożądanych (AE) wystąpiło u 4,7% pacjentów w grupie przyjmującej selperkatynib i 26,8% w grupie kontrolnej. Śmiertelne AE wystąpiły u 2,1% pacjentów w każdej grupie.
Wyniki badania LIBRETTO-531 przedstawione na Kongresie ESMO 2023 przez Dr Hadoux zostały równolegle opublikowane w The New England Journal of Medicine
źródłó:
1. Hadoux J, Elisei R, Brose MS, et al. Randomized phase III study of selperkatynib versus kabozantynib or wandetanib in advanced, kinase inhibitor-naïve, RET-mutant medullary thyroid cancer. Presented at ESMO Congress 2023. Oct 20-24, 2023. Madrid, Spain. Abstract LBA3.
2. Hadoux J, Elisei R, Brose MS, et al. Phase 3 trial of selperkatynib in advanced RET-mutant medullary thyroid cancer. N Engl J Med. Published online October 21, 2023. doi:10.1056/NEJMoa2309719 – dostęp 22 października 2023

