Badanie CheckMate 77T przedstawione w trakcie Kongresu ESMO2023 wykazało znaczącą poprawę przeżycia wolnego od zdarzeń z neoadjuwantowym niwolumabem plus chemioterapią po których następował adjuwantowy niwolumab.
Niwolumab na sesji prezydenckiej
Według wstępnych wyników z badania fazy III CheckMate 77T przedstawionych na sympozjum prezydenckim na Kongresie ESMO 2023 w Madrycie. Neoadjuwantowy niwolumab plus chemioterapia, po których następował adjuwantowy niwolumab znacząco poprawił medianę przeżycia wolnego od zdarzeń (EFS) w porównaniu z chemioterapią plus adjuwantowym placebo (nie osiągnięto w porównaniu z 18,4 miesiąca, współczynnik ryzyka 0,58; 97,36% przedział ufności [CI] 0,42–0,81; p=0,00025) przy minimalnej obserwacji 15,7 miesiąca. W badaniu wzięło udział 461 pacjentów z nieleczonym resekcyjnym niedrobnokomórkowym rakiem płuca (NDRP) w stadium IIA–IIIB, z których 77% przeszło ostateczną operację.

Wyniki badanie CheckMate 77T
Badanie CheckMate 77T (identyfikator ClinicalTrials.gov: NCT04025879) zrekrutowało pacjentów z wcześniej nieleczonym, resekcyjnym NDRP w stadium IIA-IIIB bez mutacji EGFR lub ALK i wynikami statusu funkcjonalnego ECOG 0 lub 1.
Łącznie 461 pacjentów zostało losowo przydzielonych do otrzymania schematu z niwolumabem (n=229) lub placebo (n=232). Pacjenci w ramieniu z niwolumabem otrzymywali neoadjuwantowy niwolumab (360 mg co 3 tygodnie) plus chemioterapię przez 4 cykle, po których następowała operacja i adjuwantowy niwolumab (480 mg co 4 tygodnie przez 1 rok).
Pacjenci w ramieniu kontrolnym otrzymywali neoadjuwantową chemioterapię i placebo, po których następowała operacja i adjuwantowe placebo.
Po medianie obserwacji wynoszącej 25,4 miesiąca mediana EFS nie została osiągnięta w ramieniu z niwolumabem i wynosiła 18,4 miesiąca w ramieniu z placebo (współczynnik zagrożenia, 0,58; 97,36% CI, 0,42-0,81; P =0,00025).
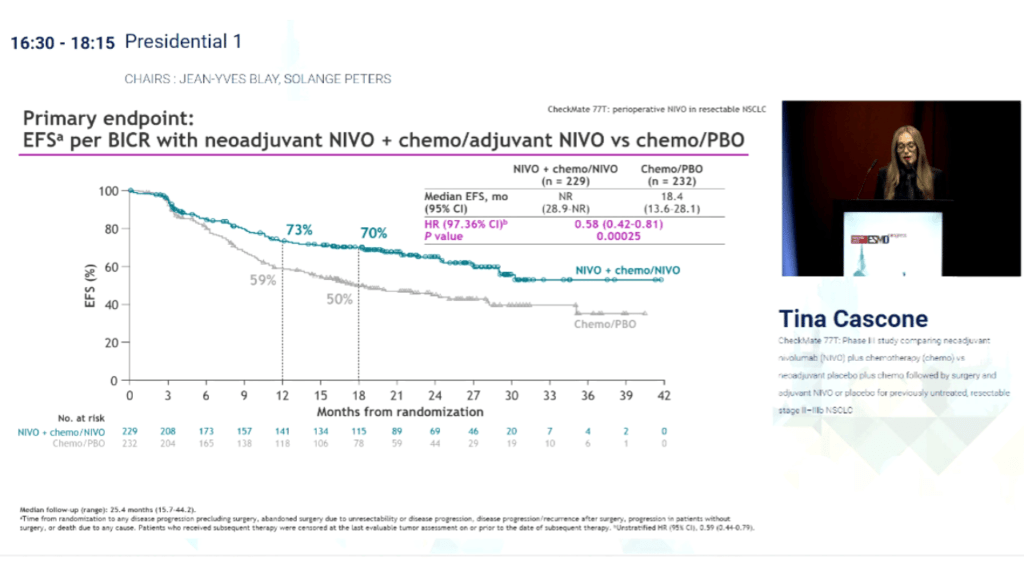
Odsetek EFS po 12 miesiącach wynosił 73% w ramieniu z niwolumabem i 59% w ramieniu z placebo. Odsetek EFS po 24 miesiącach wynosił odpowiednio 70% i 50%.
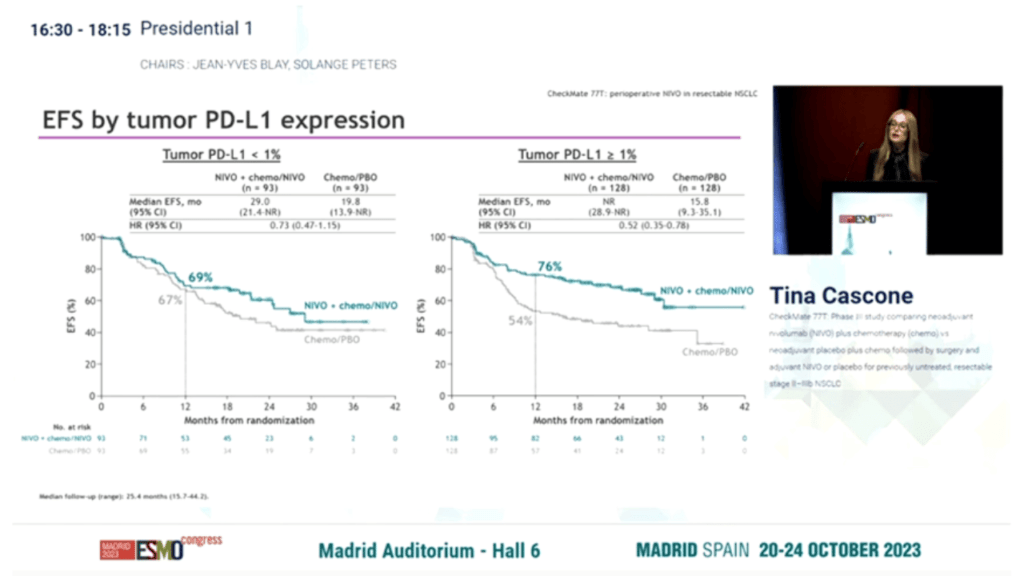
Niwolumab był również związany z poprawą wskaźników odpowiedzi. Odsetek patologicznej całkowitej odpowiedzi wynosił 25,3% w ramieniu z niwolumabem i 4,7% w ramieniu z placebo (iloraz szans [OR], 6,64; 95% CI, 3,40-12,97). Odsetek głównej patologicznej odpowiedzi wynosił odpowiednio 35,4% i 12,1% (OR, 4,01; 95% CI, 2,48-6,49).
Bezpieczeństwo niwolumabu
W całym okresie badania odsetek działań niepożądanych związanych z leczeniem (TRAEs) wynosił 89% w ramieniu z niwolumabem i 87% w ramieniu z placebo. Odsetek TRAEs stopnia 3-4 wynosił odpowiednio 32% i 25%.
W okresie neoadjuwantowym odsetek TRAEs wynosił 86% w ramieniu z niwolumabem i 85% w ramieniu z placebo. Odsetek TRAEs stopnia 3-4 wynosił odpowiednio 27% i 23%.
W okresie adjuwantowym odsetek TRAEs wynosił 50% w ramieniu z niwolumabem i 30% w ramieniu z placebo. Odsetek TRAEs stopnia 3-4 wynosił odpowiednio 8% i 3%.
W ramieniu z niwolumabem wystąpiły 2 zgony związane z leczeniem. Oba były spowodowane zapaleniem płuc i oba wystąpiły w okresie neoadjuwantowym.
Te wyniki popierają stosowanie perioperacyjnego niwolumabu jako potencjalnej nowej opcji leczenia dla pacjentów z resekcyjnym NDRP – powiedziała dr Cascone, prezentująca wyniki badań w trakcie sesji prezydenckiej Kongresu ESMO2023
Źródło:
Cascone T, Awad MM, Spicer JD, et al. CheckMate 77T: Phase III study comparing neoadjuvant nivolumab (NIVO) plus chemotherapy (chemo) vs neoadjuvant placebo plus chemo followed by surgery and adjuvant NIVO or placebo for previously untreated, resectable stage II–IIIb NSCLC. Presented at ESMO Congress 2023. Oct. 20-24, 2023. Madrid, Spain. Abstract LBA1. Dostęp 21 października 2023

